Una persona a bebido 500 cc de una bebida espirituosa conocida como Jack Daniel´s, cuya concentración es de 40 m/v de alcohol. Sabiendo que el 15% de alcohol ingerido pasa al torrente sanguíneo y que el volumen de sangre en el adulto es de 5 litros y que la concentración de alcohol considerada tóxica es de 0,003 g alcohol/en 1 ml de sangre. ¿Indicar si dicha persona se encuentra intoxicada?
AYUDA: ESTE EJERCICIO SE RESUELVE CON 3 REGLAS DE 3.
SUERTE.... =)
NOTA: Las actividades solicitadas deben enviar una fotografía al siguiente correo davidcordova30@gmail.com, para su registro, hasta el día viernes 1 de mayo, para su registro.
En este blog, encontraras valiosa información para cursos con éxito tus cursos de Ciencias Naturales en Básica superior y Química General y del Carbono, con divertidos experimentos y videos explicativos de como resolver ejercicios o cualquier duda solo escribe, y como lo dijo Benjamín Franklin: "Dime y lo olvido, enseñame y lo recuerdo, involúcrame y lo aprendo"
martes, 28 de abril de 2020
sábado, 25 de abril de 2020
domingo, 19 de abril de 2020
UNIDADES FÍSICAS DE CONCENTRACIÓN
Indica los gramos de soluto contenidos por cada 100 gramos de solución.
La solubilidad es la cantidad máxima de soluto que puede ser disuelto en un solvente en equilibrio, conformando así una solución saturada.
Las sustancias solubles son aquellas que, al entrar en contacto con otro líquido, se disuelven y forman una solución. La sustancia que se disuelve es el soluto y la sustancia en la que se disuelve es el solvente. La solución es la mezcla entre soluto y solvente.
Soluto y solvente pueden presentarse en estado líquido, sólido y gaseoso. Estos materiales o sustancias intercambian electrones al entrar en contacto en las proporciones adecuadas. Esto da lugar a la formación de nuevos compuestos. El solvente universal es el agua; sin embargo, no todos los materiales o sustancias son solubles en este elemento.

Recuperado de: http://aprendoquimik.weebly.com/unidades-de-concentracion.html
Ingresa y observa los siguientes videos:
https://www.youtube.com/watch?v=wzfGnnOqkXU
https://www.youtube.com/watch?v=eQVNU9Jo14E
para entender mejor acerca de unidades de concentración físicas, y a continuación realiza las siguientes actividades:
a) Entre los diferentes productos de tu casa, encuentra soluciones que tengan concentraciones y realiza una lista de al menos 5 productos con el porcentaje de concentración.
b) Calcule el número de gramos de agua, que deben añadirse a 8,5 gramos de cloruro de potasio, para preparar una solución acuosa de la sal al 12%.
c) Calcule el número de gramos de azúcar C12H22O11, que deben disolverse en 825 gramos de agua, para preparar una solución al 20%.
d) La densidad de una solución de Nitrato de potasio KNO3, preparara disolviendo 20 gramos de KNO3 en agua, hasta obtener un volumen final de 200 mililitros es de 1,09 g/cc. ¿Hallar el porcentaje en masa del Nitrato de potasio?
NOTA: Las actividades solicitadas deben enviar una fotografía al siguiente correo davidcordova30@gmail.com, para su registro, hasta el día viernes 24 de abril.
La solubilidad es la cantidad máxima de soluto que puede ser disuelto en un solvente en equilibrio, conformando así una solución saturada.
Las sustancias solubles son aquellas que, al entrar en contacto con otro líquido, se disuelven y forman una solución. La sustancia que se disuelve es el soluto y la sustancia en la que se disuelve es el solvente. La solución es la mezcla entre soluto y solvente.
Soluto y solvente pueden presentarse en estado líquido, sólido y gaseoso. Estos materiales o sustancias intercambian electrones al entrar en contacto en las proporciones adecuadas. Esto da lugar a la formación de nuevos compuestos. El solvente universal es el agua; sin embargo, no todos los materiales o sustancias son solubles en este elemento.

Recuperado de: http://aprendoquimik.weebly.com/unidades-de-concentracion.html
Ingresa y observa los siguientes videos:
https://www.youtube.com/watch?v=wzfGnnOqkXU
https://www.youtube.com/watch?v=eQVNU9Jo14E
para entender mejor acerca de unidades de concentración físicas, y a continuación realiza las siguientes actividades:
a) Entre los diferentes productos de tu casa, encuentra soluciones que tengan concentraciones y realiza una lista de al menos 5 productos con el porcentaje de concentración.
b) Calcule el número de gramos de agua, que deben añadirse a 8,5 gramos de cloruro de potasio, para preparar una solución acuosa de la sal al 12%.
c) Calcule el número de gramos de azúcar C12H22O11, que deben disolverse en 825 gramos de agua, para preparar una solución al 20%.
d) La densidad de una solución de Nitrato de potasio KNO3, preparara disolviendo 20 gramos de KNO3 en agua, hasta obtener un volumen final de 200 mililitros es de 1,09 g/cc. ¿Hallar el porcentaje en masa del Nitrato de potasio?
NOTA: Las actividades solicitadas deben enviar una fotografía al siguiente correo davidcordova30@gmail.com, para su registro, hasta el día viernes 24 de abril.
sábado, 18 de abril de 2020
RESPUESTAS A LA ACTIVIDAD MÉTODOS DE SEPARACIÓN DE FASES
1. Para preparar una torta, María sigue las instrucciones en
una de las cuáles se le pide que cierna 500 gramos de harina. ¿Qué método de
separación está haciendo María?
RESPUESTA: Al
utilizar un cernidor María, esta separando gránulos sólidos de diversos tamaños,
por lo tanto utiliza el método de separación TAMIZACIÓN.
2. Observa la imagen y deduce que método de separación es:

RESPUESTA: La DESTILACIÓN, es el método que se
utiliza para la separación de dos líquidos que tienen diferentes puntos de
ebullición, ya que el alcohol se evapora primero y pasa por el alambique para
su enfriamiento y recogerlo en forma líquida.
3. Lee el siguiente artículo y deduce que tipo de separación
se produce:
En el año 2010 se produjo uno de los derrames de petróleo mas grandes de la historia, sobre el Golfo de México, alrededor de 172 millones de galones de petróleo se derramaron sobre dicho Golfo, la causante seria un dispositivo de seguridad, la cual se encontraba encima de la plataforma submarina y se tenía múltiples defectos, las válvulas de ese tipo están conectadas a las tapas de los pozos petroleros submarinos. En caso de una emergencia, estos dispositivos de seguridad emplean diversos mecanismos como candados o tenazas, para detener un derrame petrolero y evitar que el petróleo surja del pozo hacia la plataforma.
En el año 2010 se produjo uno de los derrames de petróleo mas grandes de la historia, sobre el Golfo de México, alrededor de 172 millones de galones de petróleo se derramaron sobre dicho Golfo, la causante seria un dispositivo de seguridad, la cual se encontraba encima de la plataforma submarina y se tenía múltiples defectos, las válvulas de ese tipo están conectadas a las tapas de los pozos petroleros submarinos. En caso de una emergencia, estos dispositivos de seguridad emplean diversos mecanismos como candados o tenazas, para detener un derrame petrolero y evitar que el petróleo surja del pozo hacia la plataforma.
RESPUESTA: Cuando
se tiene dos líquidos que poseen diferente
densidad, podemos utilizar el método de separación DECANTACIÓN, el de menor densidad quedara flotando sobre el de
mayor densidad. Al comparar las densidades del petróleo 0,5 kg/litro y el del
agua que es 1,00 g/litro, por lo tanto el petróleo queda por encima del agua.
4. Lee el siguiente proceso y deduce que tipo de separación
se produce:
COMO HACER JUGO DE MORA
Ingredientes
- Miel a gusto
- 3 tazas de agua
- 1 taza de moras
- Hielo al gusto
- 4 hojas de hierba buena.
Preparación
- Para comenzar retira todas las hojas de las moras y lavar
muy bien las moras.
- Agregar las moras a la licuadora, junto con el agua y la
hierba buena, licuar hasta ver que el jugo es uniforme.
- Pasar el jugo por un colador, para retirar todas las
semillas de la mora.
- Volver a licuar el jugo agregando la miel.
-Listo ya tienes tu jugo, sírvelo con hielo y disfrútalo.
RESPUESTA: En el
paso para la realización del jugo de mora, al pasar el jugo por un colador se
esta separando un líquido de un sólido, por lo tanto el método de separación
que se utiliza es: FILTRACIÓN
5. Pedro esta aprendiendo a cocinar, y la receta para hacer
arroz le pide que mezcle 4 tazas de agua (1 litro), con 250 gramos de cloruro
de sodio (sal), para tener un sabor ideal. PREGUNTA: Pedro esta
haciendo una solución diluida, saturada, concentrada o sobresaturada,
reflexiona y justifica tu respuesta.
RESPUESTA: Si
leemos la información acerca de la clasificación de las soluciones: Concentradas.
La proporción de soluto respecto del solvente es grande. Ejemplo: una
disolución de 25 g de sal de mesa en 100 g de agua.
Deducimos que es una SOLUCIÓN
CONCENTRADA, ya que en la receta solo hemos aumentado por diez la concentración
del soluto con respecto al solvente.
6. De la siguiente lista realiza un cuadro de clasificación
de las soluciones e infiere lo siguiente: Estado del sistema, solvente y
soluto.
|
|
ESTADO DEL SISTEMA
|
SOLVENTE
|
SOLUTO
|
|
ACERO
|
SÓLIDO
|
SÓLIDO
|
SÓLIDO
|
|
RON CON COLA
|
LÍQUIDO
|
LÍQUIDO
|
LÍQUIDO
|
|
ESPUMA DE CARNAVAL
|
GAS
|
GAS
|
LÍQUIDO
|
|
CAFÉ
|
LÍQUIDO
|
LÍQUIDO
|
SÓLIDO
|
|
AGUA MINERAL
|
LÍQUIDO
|
LÍQUIDO
|
GAS
|
lunes, 13 de abril de 2020
MÉTODOS DE SEPARACIÓN DE FASES
Los métodos de separación de fases son procedimientos físicos y mecánicos destinados a separar las diferentes fases de una dispersión. En estos procesos las sustancias no se transforman, solo se separan. El método usado depende de las características de las fases del sistema. Por ejemplo:

Tamización. Es un método utilizado para separar dos fases sólidas con particulado de diferente tamaño, mediante un tamiz, criba o cernidor con perforaciones adecuadas para que deje pasar la fase más pequeña y
retenga la más grande. Así se separan, por ejemplo, semillas de diferentes cereales, la arena o la harina.
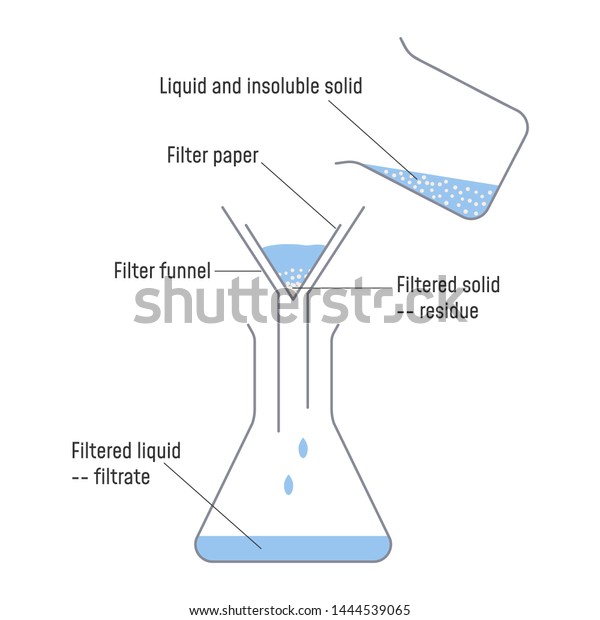
Filtración. Es un método usado para separar un sólido insoluble de un Líquido. Consiste en hacer pasar la dispersión por un filtro que retiene las partículas sólidas y deja pasar el líquido. Así se separan, por ejemplo, las impurezas de la leche en las plantas de pasteurización. En muchos casos se usan filtros prensa, como en la extracción de aceites de oliva o girasol.
 Decantación. Es el método usado para separar dos líquidos no miscibles de diferentes densidades o un sólido insoluble. Consiste simplemente en dejar el sistema en reposo durante un tiempo, de modo que la fase más densa se deposita en el fondo y la menos densa queda arriba. Así se separan, por ejemplo, las impurezas sólidas en los procesos de potabilización de aguas de río.
Decantación. Es el método usado para separar dos líquidos no miscibles de diferentes densidades o un sólido insoluble. Consiste simplemente en dejar el sistema en reposo durante un tiempo, de modo que la fase más densa se deposita en el fondo y la menos densa queda arriba. Así se separan, por ejemplo, las impurezas sólidas en los procesos de potabilización de aguas de río.
 Destilación. Usado para fraccionar soluciones de dos líquidos o de un líquido que se quiere separar de sus sólidos disueltos. Consiste en someter al sistema a la acción del calor hasta que el componente de menor punto de ebullición comience a hervir; sus vapores son conducidos a un refrigerante que los vuelve a condensar. Los dispositivos utilizados para este proceso reciben el nombre de destiladores o alambiques. Por este proceso se obtiene el agua destilada y se concentra el alcohol para las bebidas alcohólicas.
Destilación. Usado para fraccionar soluciones de dos líquidos o de un líquido que se quiere separar de sus sólidos disueltos. Consiste en someter al sistema a la acción del calor hasta que el componente de menor punto de ebullición comience a hervir; sus vapores son conducidos a un refrigerante que los vuelve a condensar. Los dispositivos utilizados para este proceso reciben el nombre de destiladores o alambiques. Por este proceso se obtiene el agua destilada y se concentra el alcohol para las bebidas alcohólicas.
Cabe mencionar que estos son los métodos más conocidos para la separación física de mezclas, mas no son los únicos.

Fuente: http://quimicamdup.blogspot.com/2013/09/soluciones-componentes-tipos-y.html
Una vez realizado la lectura de la entrada, contesta en tu cuaderno las siguientes preguntas:
1. Para preparar una torta, María sigue las instrucciones en una de las cuáles se le pide que cierna 500 gramos de harina. ¿Qué método de separación esta haciendo María?
2. Observa la imagen y deduce que método de separación es:

3. Lee el siguiente artículo y deduce que tipo de separación se produce:
En el año 2010 se produjo uno de los derrames de petróleo mas grandes de la historia, sobre el Golfo de México, alrededor de 172 millones de galones de petróleo se derramaron sobre dicho Golfo, la causante seria un dispositivo de seguridad, la cual se encontraba encima de la plataforma submarina y se tenía múltiples defectos, las válvulas de ese tipo están conectadas a las tapas de los pozos petroleros submarinos. En caso de una emergencia, estos dispositivos de seguridad emplean diversos mecanismos como candados o tenazas, para detener un derrame petrolero y evitar que el petróleo surja del pozo hacia la plataforma.
4. Lee el siguiente proceso y deduce que tipo de separación se produce:

Tamización. Es un método utilizado para separar dos fases sólidas con particulado de diferente tamaño, mediante un tamiz, criba o cernidor con perforaciones adecuadas para que deje pasar la fase más pequeña y
retenga la más grande. Así se separan, por ejemplo, semillas de diferentes cereales, la arena o la harina.
Filtración. Es un método usado para separar un sólido insoluble de un Líquido. Consiste en hacer pasar la dispersión por un filtro que retiene las partículas sólidas y deja pasar el líquido. Así se separan, por ejemplo, las impurezas de la leche en las plantas de pasteurización. En muchos casos se usan filtros prensa, como en la extracción de aceites de oliva o girasol.
 Decantación. Es el método usado para separar dos líquidos no miscibles de diferentes densidades o un sólido insoluble. Consiste simplemente en dejar el sistema en reposo durante un tiempo, de modo que la fase más densa se deposita en el fondo y la menos densa queda arriba. Así se separan, por ejemplo, las impurezas sólidas en los procesos de potabilización de aguas de río.
Decantación. Es el método usado para separar dos líquidos no miscibles de diferentes densidades o un sólido insoluble. Consiste simplemente en dejar el sistema en reposo durante un tiempo, de modo que la fase más densa se deposita en el fondo y la menos densa queda arriba. Así se separan, por ejemplo, las impurezas sólidas en los procesos de potabilización de aguas de río.Cabe mencionar que estos son los métodos más conocidos para la separación física de mezclas, mas no son los únicos.
CLASIFICACIÓN DE LAS SOLUCIONES
Dependiendo de su concentración, las disoluciones se clasifican en diluidas, concentradas, saturadas
y sobresaturadas.
Diluidas. La cantidad de soluto respecto del solvente es pequeña. Ejemplo: una solución de 1 g de sal de mesa en 100 g de agua.
Concentradas. La proporción de soluto respecto del solvente es grande. Ejemplo: una disolución de 25 g de sal de mesa en 100 g de agua.
Saturadas. Cuando la disolución no admite más cantidad de soluto disuelto. Por ejemplo, si añadimos 36 g de sal de mesa en 100 g de agua a 20º C. Si se intenta disolver 38 g de sal en 100 g de agua, solo se disolverían 36 g, y los 2 g restantes permanecerían en el fondo del vaso sin disolverse.
Sobresaturadas. Si la disolución contiene mayor cantidad de soluto que la permitida a una temperatura determinada. La sobresaturación se produce por enfriamientos rápidos o por descompresiones bruscas. Ejemplo: al sacar el corcho a una botella de refresco gaseoso.
Cuadro de tipos de soluciones según su estado de agregación.

Fuente: http://quimicamdup.blogspot.com/2013/09/soluciones-componentes-tipos-y.html
Una vez realizado la lectura de la entrada, contesta en tu cuaderno las siguientes preguntas:
1. Para preparar una torta, María sigue las instrucciones en una de las cuáles se le pide que cierna 500 gramos de harina. ¿Qué método de separación esta haciendo María?
2. Observa la imagen y deduce que método de separación es:

3. Lee el siguiente artículo y deduce que tipo de separación se produce:
En el año 2010 se produjo uno de los derrames de petróleo mas grandes de la historia, sobre el Golfo de México, alrededor de 172 millones de galones de petróleo se derramaron sobre dicho Golfo, la causante seria un dispositivo de seguridad, la cual se encontraba encima de la plataforma submarina y se tenía múltiples defectos, las válvulas de ese tipo están conectadas a las tapas de los pozos petroleros submarinos. En caso de una emergencia, estos dispositivos de seguridad emplean diversos mecanismos como candados o tenazas, para detener un derrame petrolero y evitar que el petróleo surja del pozo hacia la plataforma.
4. Lee el siguiente proceso y deduce que tipo de separación se produce:
COMO HACER JUGO DE MORA
Ingredientes
- Miel a gusto
- 3 tazas de agua
- 1 taza de moras
- Hielo al gusto
- 4 hojas de hierba buena.
Preparación
- Para comenzar retira todas las hojas de las moras y lavar muy bien las moras.
- Agregar las moras a la licuadora, junto con el agua y la hierba buena, licuar hasta ver que el jugo es uniforme.
- Pasar el jugo por un colador, para retirar todas las semillas de la mora.
- Volver a licuar el jugo agregando la miel.
-Listo ya tienes tu jugo, sírvelo con hielo y disfrútalo.
5. Pedro esta aprendiendo a cocinar, y la receta para hacer arroz le pide que mezcle 4 tazas de agua (1 litro), con 250 gramos de cloruro de sodio (sal), para tener un sabor ideal. PREGUNTA: Pedro esta haciendo una solución diluida, saturada, concentrada o sobresaturada, reflexiona y justifica tu respuesta.
6. De la siguiente lista realiza un cuadro de clasificación de las soluciones e infiere lo siguiente: Estado del sistema, solvente y soluto.
- Acero
- Dióxido de carbono
- Ron con cola
- Espuma de carnaval
- Café
- Agua mineral
NOTA: Las actividades solicitadas deben enviar una fotografía al siguiente correo davidcordova30@gmail.com, para su registro, hasta el día viernes 17 de abril.
domingo, 12 de abril de 2020
martes, 7 de abril de 2020
SISTEMAS DISPERSOS

Realize la lectura del siguiente link: https://www.lifeder.com/sistemas-dispersos/ y contesta en tu cuaderno, las siguientes preguntas:
1. Qué es un sistema disperso
2. Cuáles son los principales tipos de sistemas dispersos.
3. Cuantas fases existen en un sistema disperso.
4. Realize un cuadro de doble entrada con las semejanzas y diferencias, existentes entre un coloide, solución y una suspensión.
5. Realiza una lista con 10 productos que encuentres en tu casa, y clasificalos entre suspensión, coloide o solución.
NOTA: Las actividades solicitadas deben enviar una fotografía al siguiente correo davidcordova30@gmail.com, para su registro, hasta el día viernes 10 de abril.
Recuperado de: https://ava-bachillerato.educacion.gob.ec/mod/url/view.php?id=35030
sábado, 4 de abril de 2020
jueves, 2 de abril de 2020
Suscribirse a:
Comentarios (Atom)
CUENTOS CORTOS PARA ENTENDER QUÍMICA
EL DÍA QUE LA QUÍMICA ENGAÑO AL REGIMEN NAZI Una de las condecoraciones de mayor importancia para los científicos que han logrado ...

-
Los cálculos masa/volumen, nos indica la cantidad de gramos de soluto en 100 ml de solución. Los cálculos volumen/volumen, nos indica la ca...
-
Clase del día 18/05/2020 Recuperado de: https://quimica.laguia2000.com/general/unidades-de-concentracion-parte-1 MOLARIDAD (...