En este blog, encontraras valiosa información para cursos con éxito tus cursos de Ciencias Naturales en Básica superior y Química General y del Carbono, con divertidos experimentos y videos explicativos de como resolver ejercicios o cualquier duda solo escribe, y como lo dijo Benjamín Franklin: "Dime y lo olvido, enseñame y lo recuerdo, involúcrame y lo aprendo"
domingo, 29 de marzo de 2020
martes, 24 de marzo de 2020
viernes, 20 de marzo de 2020
jueves, 19 de marzo de 2020
miércoles, 18 de marzo de 2020
LEY DE GAY LUSSAC
FUENTE: https://sites.google.com/site/rinconcitodeciencias/quimica-decimo/el-estado-gaseoso-1/las-leyes-de-los-gases/ley-de-gay-lussac
La ley de Gay Lussac enuncia: "A un volumen constante, la presión de una masa fija de un gas es directamente proporcional a su temperatura absoluta (kelvin). Su fórmula matemática se epresa de la siguiente manera:
P1/T1 = P2/T2
Teniendo que: P1= Presión inicial
P2= Presión final
T1= Temperatura inicial
T2= Temperatura final
Ingresa y observa el siguiente video: https://www.youtube.com/watch?v=NmGo7HCEUac para entender mejor acerca de la ley de Gay Lussac, y a continuación realiza las actividades:
1. Explica mediante un ejemplo de la vida cotidiana como se cumple la ley de Gay Lussac.
2. Ejercicios:
a) La temperatura de 1 litro de un gas ideal, que inicialmente se encontraba en T.P.N, cambia a 220 grados celsius mientras que el volumen se mantiene constante. ¿Calcule la presión final del gas en torricelis?
b) Un tanque contiene gas a 20 grados farenheit y 3000 milibares. El tanque esta preparado para soportar 370 000 N/m2 (newton/metro cuadrado). Si debido a un incendio la temperatura asciende a 40 grados celsius. ¿El tanque soportara la presión, justifica tu respuesta?
NOTA: Todas las actividades de esta entrada de blog, deben ser realizadas en el cuaderno hasta el día 3 de Abril, y para evidenciar el trabajo propuesto se debe enviar una foto al siguiente correo: daviddcordova30@gmail.com
martes, 17 de marzo de 2020
LEY DE CHARLES

Fuente: https://sites.google.com/site/rinconcitodeciencias/quimica-decimo/el-estado-gaseoso-1/las-leyes-de-los-gases/ley-de-charles
El enunciado de la ley de Charles dice: "A presión constante, el volumen ocupado por una masa definida de una muestra de un gas, es directamente proporcional a la temperatura absoluta (kelvin). Teniendo que la fórmula matemática queda de la siguiente manera:
V1/T1 = V2/T2
Teniendo que: V1= Volumen inicial
V2= Volumen final
T1= Temperatura inicial
T2= Temperatura final.
Ingresa y observa el siguiente video: https://www.youtube.com/watch?v=x3FAkm8_Ur0 para profundizar acerca de la ley de Charles, y a continuación realiza las actividades:
1. Explica mediante un ejemplo de la vida cotidiana como se cumple la ley de Charles.
2. Ejercicios:
a) 10 gramos de cloro molecular, se encuentran en un recipiente de 22 litros a 30 grados farenheit.¿Cuál es la temperatura del gas en kelvin, cuando se pasa a un recipiente de 3000 centímetros cúbicos?
b) Una muestra de gas ocupa un volumen de 160 mililitros a 1 atmósfera de presión y 27 grados celsius. ¿Calcular el nuevo volumen a 5 grados celsius y 760 mmHg?
NOTA: Todas las actividades de esta entrada de blog, deben ser realizadas en el cuaderno hasta el día 27 de Marzo , y para evidenciar el trabajo propuesto se debe enviar una foto al siguiente correo: daviddcordova30@gmail.com
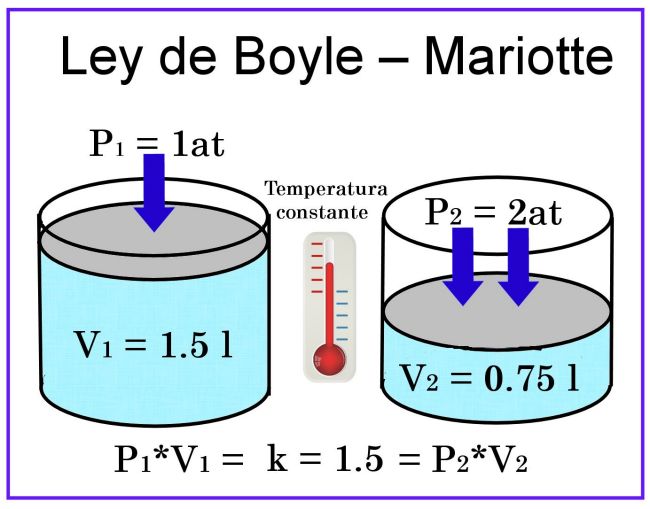
LEY DE BOYLE
El enunciado de la Ley de Boyle de los gases es:
A temperatura constante (k), el volumen de un gas es inversamente proporcional a la presión que es ejercida sobre él. Teniendo que la fórmula matemática es:
V1/V2 = P2/P1
En la cuál: V1= Volumen inicial
V2= Volumen final
P1= Presión inicial
P2= Presión final
En el siguiente link, encontraras ejercicios para entender mejor acerca de la ley de Boyle.
En tu cuaderno de Química General, desarrolla las siguientes actividades:
1. Mediante un ejemplo de la vida cotidiana, explica como se cumple la ley de Boyle.
2. Ejercicios:
a) ¿A que presión se debe someter una muestra de gas a temperatura constante para comprimirlo a de 2000 centímetros cúbicos a 800 mililitros, si su presión es de 1200 mmHg?
b) A presión de 17 atmósferas, 34 litros de un gas, a temperatura constante experimenta un cambio ocupando un volumen de 1500 centímetros cúbicos. ¿Cuál sera la presión que se ejerce?
NOTA: Los ejercicios deben ser presentados hasta el día viernes 20 de marzo, mediante una fotografía al siguiente correo: daviddcordova30@gmail.com
Suscribirse a:
Comentarios (Atom)
CUENTOS CORTOS PARA ENTENDER QUÍMICA
EL DÍA QUE LA QUÍMICA ENGAÑO AL REGIMEN NAZI Una de las condecoraciones de mayor importancia para los científicos que han logrado ...

-
Los cálculos masa/volumen, nos indica la cantidad de gramos de soluto en 100 ml de solución. Los cálculos volumen/volumen, nos indica la ca...
-
Clase del día 18/05/2020 Recuperado de: https://quimica.laguia2000.com/general/unidades-de-concentracion-parte-1 MOLARIDAD (...