El enunciado de la Ley de Boyle de los gases es:
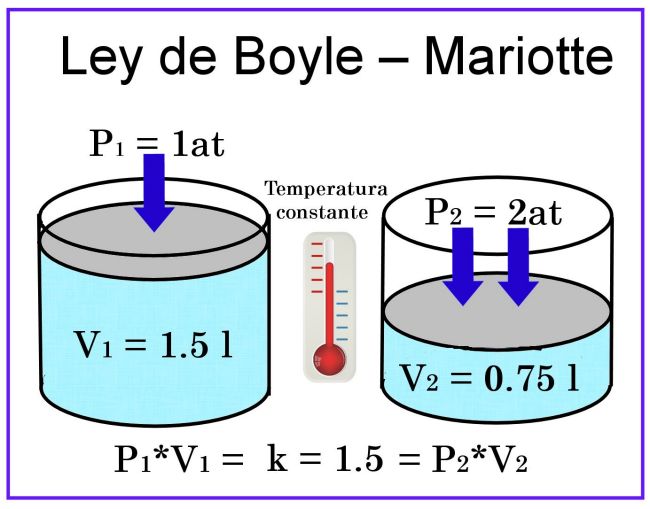
A temperatura constante (k), el volumen de un gas es inversamente proporcional a la presión que es ejercida sobre él. Teniendo que la fórmula matemática es:
V1/V2 = P2/P1
En la cuál: V1= Volumen inicial
V2= Volumen final
P1= Presión inicial
P2= Presión final
En el siguiente link, encontraras ejercicios para entender mejor acerca de la ley de Boyle.
En tu cuaderno de Química General, desarrolla las siguientes actividades:
1. Mediante un ejemplo de la vida cotidiana, explica como se cumple la ley de Boyle.
2. Ejercicios:
a) ¿A que presión se debe someter una muestra de gas a temperatura constante para comprimirlo a de 2000 centímetros cúbicos a 800 mililitros, si su presión es de 1200 mmHg?
b) A presión de 17 atmósferas, 34 litros de un gas, a temperatura constante experimenta un cambio ocupando un volumen de 1500 centímetros cúbicos. ¿Cuál sera la presión que se ejerce?
NOTA: Los ejercicios deben ser presentados hasta el día viernes 20 de marzo, mediante una fotografía al siguiente correo: daviddcordova30@gmail.com


♥
ResponderEliminar